去日本旅游观光,海外游客免不了到各大免税店或药妆店大采购。日本的药妆店除了医药品、化妆品之外,还销售各种各样的保健品,比如软骨素、纳豆精、鲛肝油等。
保健品在日本也被称作健康食品,因其种类繁多,且部分产品兼具疾病预防和营养补充的作用,时常令人将其与药品相混淆。以日本国宝级全营养补充剂“美妥(MICRODIET)”为例,“美妥”含有大量的蛋白质及各种微量元素,一直被世界各地的健身人士视作控制卡路里和补充营养的佳品;同时,“美妥”近20年来又一直被日本糖尿病协会和减重协会联合推广,作为糖尿病和肥胖症人群的膳食替代,在日本各大药店均有售。因此“美妥”的品牌心智常兼具保健品和药品之间。

不过,日本海关对于药品和保健品的入境规定是迥然不同的,拟出海日本的中资保健品企业而言,应首先明确日本药品和保健品的分类标准,以及其适用的法律法规,从而为企业产品的顺利进口和后续目标客群的定位提供保障。
和君咨询携手富穆咨询、沙利文,三方联手撰写了《品牌出海赴日操作手册》共上、下两册。本文摘录了关于保健品进口日本的部分内容,详细讲述了日本保健品与药品的分类标准以及涉及的法律法规差异,为中资企业打开了解的窗口。愿各位出海的企业家顺利进入日本市场。
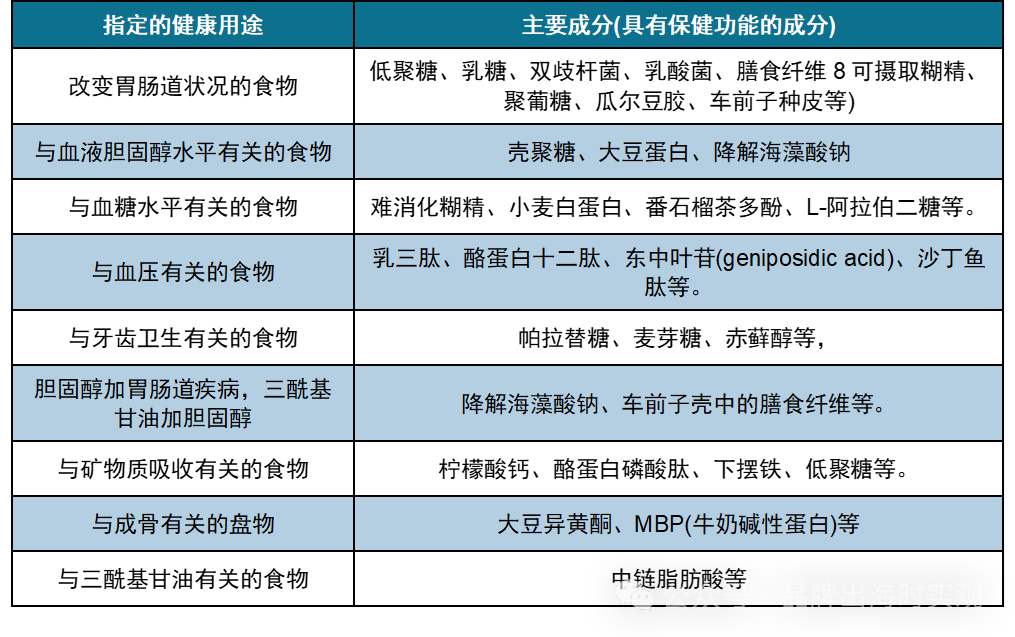
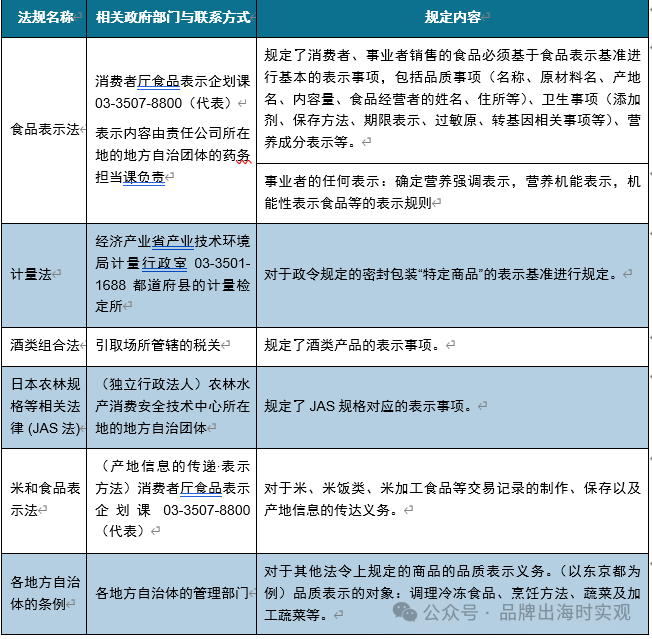
01 日本食品与药品的区分 “药品”是根据药品医疗器械等法(药品、医疗器械等的质量、有效性及安全性保障等相关法律的简称)定义的,包括以下两种: ① 旨在用于诊断、治疗或预防疾病的物品; ② 旨在影响身体结构或功能的物品。 “食品”指的是根据食品卫生法规制的、所有可食用的物品,不包括药品医疗器械等法规定的药品、非处方药品和再生医疗产品等。 在外国的健康食品或补充剂中,有些可能包含在日本被视为药品成分的物质,或标示有类似药品的功效效果,将这些产品作为食品进口和销售,将被视为“未经批准的药品”,成为药品医疗器械等法指导和监管的对象。判断食品和药品分类的标准,需要考虑以下四个要素,如果被判定为“药品”,则不能作为食品进口: 物品的成分本质(原材料) 原材料是判断进口食品是否为药品的标准之一。企业可参照日本“食品和药品分类列表”,如果成分被分类在“主要作为药品使用的成分本质列表”中,则应视为药品。 物品上标示的功效 如果商品的容器、包装、附带文件、传单、小册子、互联网等广告中明确或暗示产品具有治疗或预防疾病的功效,或增强或促进身体组织功能的一般功效,无论是否用外语标示,都视为药品。 形状(剂型、容器、包装、设计等) 例如安瓿剂、舌下锭、填充喷雾剂等,都视为药品。 物品上标示的用法用量 如果产品详细标示了服用时间、间隔、服用量等用法用量,都视为药品。 02 日本健康食品与一般性食品的分类 根据日本厚生劳动省对食品的定义,食品具有以下三大功能,分别是:为维持人类生命提供营养的第一功能(即营养功能);通过食品的味道、香气、外观等吸引人类感官的第二功能;涉及调节生物节律、抑制老化、预防生活习惯病和疾病恢复等的第三功能。 关于食品的第三功能的相关表示,被称为“功能性声明”,也是鉴别健康食品和一般性食品的重要标准,未具备第三功能的食品为“一般性食品”,反之则为“保健功能食品”,是健康食品的分支之一,除保健功能食品之外,健康食品还包括特殊用途食品,特殊用途食品是针对部分特殊人群推出的食品,如婴幼儿、孕产妇、吞咽困难者等,本文我们主要讨论的事保健功能食品。 保健功能食品又可分为特定保健用食品(FOSHU)、营养机能食品(FNFC)和功能性标示食品(FFC),如下所示,三者的监管政策和审批程序各不相同: FOSHU FOSHU的监管政策最严格,产品需要经过消费者委员会、食物安全委员会和厚生劳动省三个机构审批,可标记为单一化健康目的(如补钙)。 FOSHU的推出主要是为了应对饮食方式带来的慢性疾病。在老龄化的背景下,日本心血管疾病的死亡率很高,几乎与癌症相同,同时,自1970年代以来逐渐西化的饮食方式,也为日本国民带来较高的心血管疾病、肥胖、糖尿病和高血压的风险。因此,日本厚生劳动省于1991年制定了“特定保健用途食品”(FOSHU)作为“功能性食品”的监管制度。 图表1:日本厚生劳动省 FOSHU 许可标志及指定健康用途 资料来源:厚生劳动省 FNFC FNFC的原料监管最严格,可用成分仅 20 种,包含13种维生素、6种矿物质和1种脂肪酸,主要为补充日常饮食摄取不足的营养成分。虽然FNFC的原料监管较严格,但由于其功能已经过科学证据证实,因而在保证产品符合规范后,无需进行审批或注册,可直接在产品上标示营养成分并指定每日摄入量(如 XX 原料,xx 毫克/天)。 FFC 功能性标示食品FFC在2015年提出,监管政策、原料限制上均较FOSHU更灵活。为提振需求,2015年,日本根据美国的《膳食补充剂健康与教育法案》(DSHEA)建立了名为“功能性标示食品 FFC”的新系统。相比FOSHU,FFC的健康声明和临床研究有以下不同: 一、FFC健康声明的结构化程度提升,涵盖范围扩大: 与FOSHU相比,FFC的健康声明更灵活,并且不需要消费者厅批准,因此有较多创新。 ①首先,是功能健康声明的结构化。FOSHU的标示较为单一,一般仅指向产品的特定作用,FFC的标示更多样化、结构化,可以包含FOSHU产品对应作用的多种功能。如FOSHU中的健康声明“补钙”对应FFC中可标示为“骨骼功能”或“膝关节功能”。 ②其次,健康声明的范围扩大。FOSHU系统中的大多数健康声明,都与胃肠道或与生活方式相关的疾病代谢综合征的早期阶段有关,例如脂肪酸摄取,血清甘油三酯的控制,血糖和胆固醇的控制以及高血压的改善,通常被认为与我们的健康密切相关。在FFC中,不仅涉及FOSHU的健康声明,还涉及与皮肤、眼睛、精神压力、关节、记忆、睡眠、骨骼、疲劳、循环、体温、肌肉、肝脏、行走、背痛和其他功能有关的其他健康声明。 二、FFC临床研究更灵活,大大降低认证门槛: FOSHU和新型功能食品都需要来自临床研究的大量证据,但FOSHU的临床研究要求比FFC更严谨,从而使得FFC的认证门槛相对FOSHU大大降低,主要体现在以下三个方面。 ①研究设计:FOSHU的临床研究在目标受试者、症状参数等方面均有更高的要求; ②原理解释:在FOSHU系统的临床试验中,除了显著性外,还需要明确的证据来解释活性成分的作用方式以及用于这些成分的分析方法。相比之下,FFC的临床研究仅需显示出相对安慰剂的显著效果; ③配方变更:如果FOSHU产品的配方发生变化,则需要在FOSHU系统中为新配方提供新的临床结果。但对FFC产品而言,如果在先前的研究中已经收集了临床证据,则无需进行额外的临床研究。 三种保健功能食品的对比详见下图: 图表 2 三种保健功能食品的对比 资料来源:艾瑞咨询,和君、富穆整理 03 保健功能食品所涉及的法律法规 如果产品判定为保健功能食品,则主要涉及《食品卫生法》,需要根据食品卫生法的规格基准,对食品做有毒有害物质,安全性确认并申报检疫。作为食品大类中的保健功能食品,适用于以下法律法规: 图表 3 日本食品相关法律法规 资料来源:厚生劳动省 此外,在销售食品时,还需根据健康增进法和资源有效利用法的相关规定,禁止在宣传时存在虚假、夸大和误导性表示。 图表 4 禁止虚假、夸大和误导性表示的主要法律法规 资料来源:厚生劳动省 咨询处: 关于食品表示法的一般问题,可咨询消费者厅食品表示规划科(TEL:03-3507-880) 关于个别商品的问题,可咨询负责表示内容的公司总部所在地的保健所,通过消费者厅网站“食品表示法咨询受理窗口(各都道府县)” 链接:https://www.caa.go.jp/policies/policy/food_labeling/information/contact/prefectures/ 小结: 中国保健品出口日本时,应首先根据产品的原材料、功效、形制和用法用量四个标准判断其是否为药品,日本药品受药品医疗器械等法的监管,在研发、批准、生产、流通和使用的各个阶段均受到严格的管控,因而对于被判别为药品的保健品,进口日本将变得尤为困难。 如果产品判定为保健功能食品,则主要涉及《食品卫生法》,需要根据食品卫生法的规格基准,对食品做有毒有害物质,安全性确认并申报检疫。但需要注意的事,保健功能食品在日本可分为三种类型,分别为FOSHU、FNFC和FFC,三者的监管政策和审批方式存在较大差距,企业需根据日本消费者事务厅的相关要求进行及时注册和备案,并根据规定对产品的成分和用量进行标注。